Ультразвуковая диагностика сегодня широко используется в медицине и входит в стандарты оказания медицинской помощи при большом перечне заболеваний. Инфекции, связанные с проведением ультразвуковых исследований (УЗИ), в нашей стране не выявлялись и не регистрировались, их закономерности не изучались, что тормозило разработку профилактических мероприятий. В то же время международные клинические рандомизированные исследования доказали наличие рисков инфицирования пациентов в отсутствие оптимальных стандартов обработки датчиков. По данным P. Cervini и соавт. [1], общая частота инфекционных болезней, связанных с УЗИ, составляет 0,1%. Она может возрастать до 0,19% после трансбронхиальной тонкоигольной аспирационной биопсии под ультразвуковым контролем [2] и до 4,29% после трансректальной биопсии предстательной железы [3]. S. Leroy и соавт. [4] при помощи компьютерного моделирования и математического анализа на основе систематического обзора инфекционной заболеваемости 4 000 000 пациентов, которым проводили УЗИ, установили, что вероятность их инфицирования от контаминированных датчиков колебалась от 1 до 6% в зависимости от возбудителя. В случае ВИЧ-инфекции это могло привести к 60 инфицированным пациентам в год. Число новых случаев других распространенных вирусных инфекций может колебаться от 1600 до 15 000 в год [4]. Передача ВИЧ, вирусов гепатитов В и С при УЗИ крайне редка [5]. Описаны случай инфицирования пациентов вирусом гепатита С при трансректальной биопсии предстательной железы [6] и 2 случая – при подготовке пациенток к процедуре ЭКО [7]. В 2010 г. G. Kac и соавт. [8] и в 2012 г. J.S. Casalegno и соавт. [9] установили наличие вируса папилломы человека (ВПЧ) на вагинальных и ректальных датчиках. J.S. Casalegno и соавт. [9] показали постоянную персистенцию онкогенных ВПЧ на трансвагинальных датчиках, которые между пациентами подвергали дезинфекции низкого уровня и использовали с одноразовыми покрытиями. В 2014 г. F. M’Zali и соавт. [10] на датчиках, прошедших дезинфекцию низкого уровня, выявили признаки значительной контаминации микроорганизмами: ДНК ВПЧ была обнаружена на 13% из них (на 7% в нуклеазорезистентной форме). ДНК C. trachomatis была обнаружена методом первичной ПЦР на 20% датчиков, но только на 2% после обработки нуклеазой, в то время как ДНК микоплазмы была амплифицирована на 8 и 4% датчиков соответственно. Комменсальная микрофлора и/или бактериальная флора окружающей среды присутствовала на 86% датчиков в количестве от 10 до более 3 000 КОЕ/датчик, золотистый стафилококк выявили на поверхностях 4% датчиков в количестве от 10 до 560 КОЕ/датчик. Грибы не были выделены [10].
Зарегистрированы крупные вспышки бактериальных инфекций, связанные с неэффективно обработанными чреспищеводными и ректальными датчиками, направляющими для игл и самими иглами для проведения трансректальных биопсий [11–14].
При отсутствии нормативов и рекомендаций врачи ошибочно подменяют обработку внутриполостных датчиков использованием одноразовых стерильных и нестерильных покрытий, которые повреждаются в 0,9–13,0% случаев [11, 13, 15]. До 5% покрытий после использования имеют загрязнения кровью внутренних поверхностей [16], что косвенно подтверждает их проницаемость и возможность микроповреждений.
Профильные международные и национальные организации, такие как Всемирная федерация ультразвука в медицине и биологии (WFUMB), Европейская федерация ассоциаций ультразвука в медицине и биологии (EFSUMB), Европейское общество радиологов (ESR), Американский институт ультразвука в медицине (AIUM), Австралийское общество ультразвука в медицине (ASUM), Израильское общество ультразвука в медицине (ISDUM), Британское медицинское ультразвуковое общество (BMUS), сформулировали требования инфекционного контроля в ультразвуковой диагностике [17–22]. В нашей стране требования к обеспечению эпидемиологической безопасности ультразвуковых методов диагностики не были разработаны. Российская ассоциация специалистов ультразвуковой диагностики в медицине (РАСУДМ) рекомендовала своим специалистам во время пандемии COVID- 19 ориентироваться на рекомендации WFUMB, которые были переведены в начале пандемии [23].
Цель исследования – обоснование необходимости разработки системы эпидемиологической безопасности ультразвуковой диагностики.
Задачи исследования:
- оценить эпидемиологическую безопасность ультразвуковой диагностики путем анкетирования врачей ультразвуковой диагностики;
- выявить основные факторы риска инфицирования пациентов.
Материалы и методы
Для выполнения работы использовали психологический вербально-коммуникативный метод. Совместно с РАСУДМ в феврале 2020 г. проведено анкетирование специалистов ультразвуковой диагностики по вопросам обеспечения эпидемиологической безопасности на платформе Google Forms. Опросник составлен специалистами Московского НИИ эпидемиологии и микробиологии им. Г.Н. Габричевского и одобрен исполнительным комитетом РАСУДМ. Он содержал 21 вопрос, касающийся обработки ультразвуковых датчиков и использования одноразовых покрытий на них. Проанализированы материалы, полученные от 869 врачей, 547 (63,0%) из которых работают в государственных и 322 (37,0%) – в частных медицинских организациях 77 административных территорий страны. Кроме того, проведено сравнение материалов, полученных из 3 регионов (Москва, Московская область, Санкт-Петербург), представленных наибольшим числом респондентов – 169, 61 и 35 соответственно. Закрытые (структурированные) вопросы предполагали выбор ответа из списка. Вопросы в анкете логически взаимосвязаны. Ответы на вопросы верхнего уровня получали подтверждения ответами на вопросы нижнего уровня. Эта цепочка позволяла оценить правильность ответов и проводить отбраковку анкет либо ответов на блок вопросов. При проведении анализа было установлено, что чрескожные, внутриполостные и интраоперационные УЗИ проводят 753 (86,6%), 629 (72,3%) и 65 (7,4%) специалистов ультразвуковой диагностики соответственно. Часть респондентов пропустили некоторые вопросы или дали на них противоречивые ответы. Такие анкеты были исключены из анализа данных разделов.
Для статистической обработки данных использовали программу MedCalc Statistical Software version 19.2.6 (MedCalc Software Ltd., Бельгия). Параметры представлены в виде абсолютных и относительных (%) значений. Сравнение достоверности различий проведено с помощью критерия χ2. Различия считались достоверными при р < 0,05.
Результаты
Варианты алгоритмов обработки чрескожных датчиков и использования покрытий для них врачами ультразвуковой диагностики в нашей стране представлены в табл. 1. Анкеты 30 респондентов были исключены из анализа по указанным выше причинам.
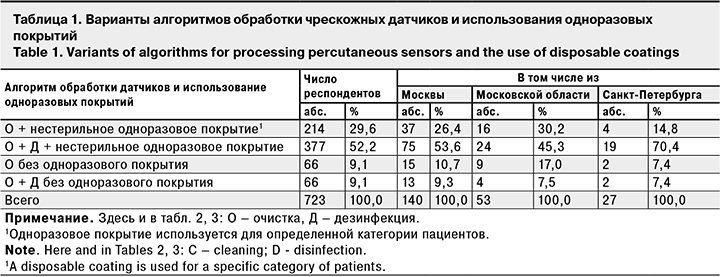
Анализ результатов показывает, что при проведении чрескожных УЗИ в 280 (38,7%) из 723 случаев имеют место потенциальные риски инфицирования пациентов, так как датчики между пациентами не дезинфицируются. В Москве не обеззараживают датчики 37,1% профильных специалистов, в Санкт-Петербурге – 22,2%, в Московской области – 47,2% (различия между регионами недостоверны). Отказ от дезинфекции датчиков способствует сохранению и накоплению на них микроорганизмов. В публикации T. Sartoretti и соавт. [24] показано, что бактериальное загрязнение необеззараженных чрескожных датчиков значительно выше, чем сидений общественного туалета и автобусных поручней.
Одноразовое покрытие для чрескожных датчиков использовал 591 (81,7%) из 723 специалистов при проведении УЗИ пациентам с инфекционным процессом кожи или наружных половых органов (при сравнении этого показателя по 3 регионам различия недостоверны). В остальных 132 случаях одноразовые покрытия никогда не используются. В 66 случаях датчики между пациентами не дезинфицируют, что повышает риски инфицирования не только для пациента, но и для медицинского персонала. Доля случаев отсутствия дезинфекции при неиспользовании одноразового покрытия была самой высокой в Московской области – 17,0%, однако при сравнении показателей 3 регионов достоверные различия не выявлены (сравнение проводили среди респондентов, не использующих одноразовые покрытия). Надо отметить, что в 29,6% случаев при чрескожных исследованиях инфицированных пациентов дезинфекция чрескожного датчика подменяется использованием одноразового нестерильного покрытия.
Варианты обработки датчиков для внутриполостных исследований и использования для них одноразовых покрытий представлены в табл. 2. Из анализа были исключены анкеты 2 респондентов.
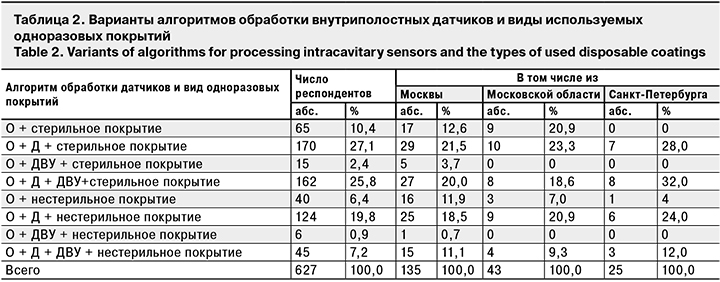
В соответствии с международной классификацией медицинских изделий по рискам их использования для пациентов внутриполостные ультразвуковые датчики относятся к полукритическим изделиям и подлежат очистке или очистке при совмещении с дезинфекцией, а также дезинфекции высокого уровня (ДВУ) [23].
При анализе материалов анкетирования выявлены 4 действующих алгоритма обработки внутриполостных датчиков. Такое многообразие вызвано отсутствием единого национального стандарта. Все представленные алгоритмы в обязательном порядке включают удаление ультразвукового геля и очистку датчика от биологических загрязнений. Это связано с тем, что остатки геля, как и биологические загрязнения, могут ограничить эффективность последующей дезинфекции [23]. Гель, как правило, удаляют сухой или влажной мягкой салфеткой. Последующую очистку как самостоятельный процесс или при совмещении с дезинфекцией проводят способами протирания или неполного погружения в раствор моющего/дезинфицирующего средства.
Только 2 алгоритма обработки из 4 проанализированных (очистка + ДВУ, очистка + дезинфекция + ДВУ) могут обеспечить инфекционную безопасность внутриполостного датчика при условии качественной очистки и корректного применения эффективных дезинфицирующих средств. Их используют 228 (36,4%) специалистов. Наиболее благоприятная обстановка в Санкт-Петербурге (44,0%), наименее – в Московской области (27,9%). Но при сравнении 3 регионов достоверные различия также не выявлены.
Необходимо отметить, что из 228 специалистов ультразвуковой диагностики, заявивших о проведении ДВУ, только 101 (44,3%) использует для этого зарегистрированные в РФ установки на основе ультрафиолетового излучения и паров пероксида водорода или химические средства, которые могут обеспечить этот уровень дезинфекции. Таким образом, реально внутриполостные датчики подвергают ДВУ на финальной стадии обработки только 16,1% специалистов.
Рейтинг основных причин, препятствующих проведению ДВУ внутриполостных датчиков, выглядит следующим образом (при допустимости нескольких ответов):
1) отсутствие условий и времени для проведения ДВУ датчика способом погружения в стерилизующее средство – 388 (61,9%) из 627 ответов;
2) отсутствие нормативных документов по обработке внутриполостных датчиков – 326 (52,0%);
3) отсутствие разрешенных санитарным законодательством новых эффективных и быстрых методов ДВУ – 221 (35,2%);
4) недостаточные знания у врачей по данному вопросу – 202 (32,2%).
Все указанные причины неразрывно связаны и вытекают друг из друга. В настоящее время технология ДВУ нормативно разрешена для эндоскопов (СП 3.1.3263-15), предназначенных для проведения нестерильных вмешательств, в том числе ультразвуковых видеоэндоскопов (видеоэндоскопы с ультразвуковым датчиком на дистальном конце вводимой трубки). Для остальных внутриполостных датчиков нашим законодательством допускается проведение только дезинфекции без указания ее уровня, что приводит к применению средств с ограниченной антимикробной активностью (четвертичные аммониевые соединения, полигексаметилен гуанидин) и возникновению неоправданных рисков инфицирования пациентов. Именно ДВУ рекомендуется WFUMB [23] и производителями зарегистрированных на территории РФ ультразвуковых аппаратов в качестве финального этапа обработки внутриполостных датчиков. В соответствии с законодательством РФ (СП 3.1.3263-15), ДВУ может быть выполнена только в растворе химического средства с последующим ополаскиванием и сушкой. Для ее выполнения требуются место (площадь), соответствующее техническое оснащение и материальное обеспечение, а также время (минимально 15–20 мин). Выполнение ДВУ врачом неизбежно приведет к кратному сокращению числа обследованных пациентов.
В РФ в установленном порядке зарегистрированы установки для проведения ДВУ ультразвуковых датчиков на основе ультрафиолетового излучения и паров пероксида водорода с коротким циклом, а также система спороцидных салфеток. Однако эти методы обработки не внесены в нормативные документы и не могут применяться для данной цели. Таким образом, в отсутствие нормативных документов по обработке ультразвуковых датчиков, а также приемлемых (быстрых и эффективных) методов ДВУ задача обеспечения эпидемиологической безопасности внутриполостных исследований не может быть решена кардинально.
Из табл. 2 следует, что только очистку и дезинфекцию внутриполостных датчиков проводят 294 (46,9%) специалиста. К ним целесообразно присоединить 117 специалистов, декларировавших ДВУ, но не обеспечивающих ее достижения. В итоге получится, что очистка и дезинфекция внутриполостных датчиков выполняются в 411 (65,6%) случаях.
Охват дезинфекцией и ДВУ внутриполостных датчиков в стране составляет 83,3%, а в 3 сравниваемых административных территориях колеблется от 72,1% (Московская область) до 96,0% (Санкт-Петербург) (различия между 3 регионами недостоверны).
Анализ средств для обеззараживания датчиков позволил выявить доминирование комбинированных средств дезинфекции с моющими свойствами, позволяющих проводить очистку при совмещении с дезинфекцией. Однако 241 (37,2%) %) из 648 респондентов использует для дезинфекции растворы альдегидов и спиртов, которые обладают выраженными фиксирующими свойствами. Для обеспечения их эффективности необходимо предварительно провести тщательную очистку.
Из возможных способов дезинфекции внутриполостных датчиков чаще всего используют протирание салфетками, смоченными в растворе химического средства. Если дезинфицирующее средство обладает моющими свойствами, процесс очистки проводят при совмещении с дезинфекцией. Менее распространено применение дезинфицирующих средств методом орошения, так как перед его выполнением датчик необходимо тщательно очистить, ополоснуть и высушить.
Высокие риски инфицирования пациентов при внутриполостных исследованиях выявлены в тех случаях, когда датчики между пациентами не обеззараживают, а проводят только их очистку (16,8%). Это случаи, когда врачи процесс дезинфекции ошибочно заменяют использованием одноразового покрытия (стерильного только в 61,9% случаев). Опубликованные работы наглядно демонстрируют высокий уровень контаминации датчиков условно-патогенными и патогенными микроорганизмами [25], а также свидетельствуют о проницаемости покрытий и вероятности их повреждения [15].
Установлено, что при проведении каждого внутриполостного УЗИ одноразовые покрытия на датчик используют 608 (97,0%) респондентов. 19 (3,0%) используют их эпизодически (при наличии покрытий или у инфицированных пациентов). При этом 412 (65,7%) специалистов отметили, что надевают на датчик стерильное покрытие, а 215 (34,3%) – нестерильное (см. табл. 2). Показатель использования стерильных одноразовых покрытий для внутриполостных датчиков при проведении каждого внутриполостного УЗИ в 3 сравниваемых регионах ниже общероссийского (65,7%): в Москве –57,8%, в Московской области – 62,8%, в Санкт-Петербурге – 60,0% (различия между регионами недостоверны). Вопрос о микробиологической чистоте одноразовых покрытий для внутриполостных датчиков очень важен, так как в процессе производства и упаковки нестерильных покрытий полностью исключить вторичную контаминацию их поверхностей невозможно.
Проанализированы анкеты 54 из 65 респондентов, выполняющих интраоперационные УЗИ. Не дали ответы на вопросы этого блока 11 респондентов. Анализ по регионам не проводили из-за незначительной выборки.
Было установлено, что после снятия стерильного покрытия ультразвуковой датчик очищают от геля салфеткой с водой или моющим средством 38 (70,4%) из 54 специалистов, 16 (29,6%) проводят очистку только сухой салфеткой.
35 (64,8%) из 54 специалистов предстерилизационную очистку датчика проводят при совмещении с дезинфекцией способом протирания, 14 (25,9%) – способом неполного погружение в раствор дезинфицирующего средства. В 5 (9,3%) случаях предстерилизационная очистка не совмещается с дезинфекцией, а предшествует ей. При этом для дезинфекции используют способ орошения, который не является для данной цели способом выбора, так как не гарантирует контакта средства дезинфекции со всеми поверхностями датчика.
На финальной стадии обработки специализированные и неспециализированные ультразвуковые датчики, используемые для интраоперационных исследований (интраоперационные датчики), подвергают стерилизации 7 (13,0%), а ДВУ разными методами – 20 (37,0%) респондентов. Стерилизацию и ДВУ неполным погружением в раствор или готовое к применению стерилизующее средство выполняют 18 (33,3%) респондентов. ДВУ способом протирания спороцидными салфетками осуществляют 7 (13,0%) респондентов, а воздействием ультрафиолетового излучения в предназначенной для этой цели установке – 2 (3,7%). Только дезинфекцию способом протирания или орошения проводят 27 (50,0%) специалистов. Таким образом, в 50,0% случаев эпидемиологическая безопасность интраоперационных исследований не может быть гарантирована.
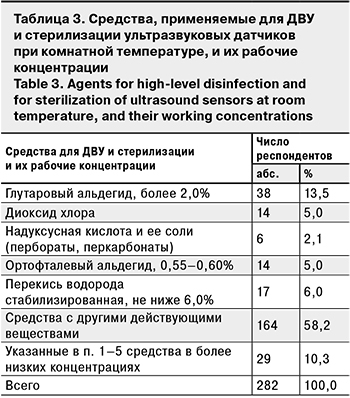 На вопрос о средствах ДВУ и стерилизации, которые применяются на финальной стадии обработки внутриполостных и интраоперационных датчиков, ответили 282 специалиста. Анализ этих средств и их рабочих концентраций (табл. 3) показал, что обеспечить ДВУ и стерилизацию датчиков могут только 89 (31,6%) из них (п. 1–5). Остальные средства (п. 6 и 7) не обладают спороцидной активностью, поэтому не могут обеспечить требуемый уровень обеззараживания. Датчики, продезинфицированные/простерилизованные этими средствами, будут инфекционно опасными.
На вопрос о средствах ДВУ и стерилизации, которые применяются на финальной стадии обработки внутриполостных и интраоперационных датчиков, ответили 282 специалиста. Анализ этих средств и их рабочих концентраций (табл. 3) показал, что обеспечить ДВУ и стерилизацию датчиков могут только 89 (31,6%) из них (п. 1–5). Остальные средства (п. 6 и 7) не обладают спороцидной активностью, поэтому не могут обеспечить требуемый уровень обеззараживания. Датчики, продезинфицированные/простерилизованные этими средствами, будут инфекционно опасными.
Одноразовые стерильные покрытия на интраоперационные датчики используют на каждую операцию 49 (90,7%) специалистов, остальные 5 (9,3%) используют покрытия при их наличии. В качестве такого покрытия 30 специалистов используют стерильный презерватив, 24 – рекомендованное производителем датчика стерильное одноразовое покрытие.
На вопрос о препятствиях в обеспечении стерильности интраоперационного датчика в операционной ране ответили 54 респондента. Результаты были следующими (при допустимости нескольких ответов):
1) препятствий для проведения ДВУ/стерилизации нет – 19 (35,2%) ответов;
2) отсутствие нормативных документов по обработке интраоперационных датчиков – 27 (50,0%);
3) отсутствие условий для ДВУ/стерилизации датчика в операционном блоке – 26 (48,1%);
4) отсутствие стерильного геля в одноразовых упаковках – 21 (38,9%);
5) недостаточное количество одноразовых стерильных покрытий – 17 (31,5%);
6) недостаточно знаний/подготовки персонала по этому вопросу – 15 (27,8%).
Очевидно, что ответы на вопрос о препятствиях в обеспечении стерильности датчика в операционной ране вошли в некоторое противоречие с ответами на вопросы по обработке самих датчиков. Они высветили реальные проблемы, в основе которых лежит отсутствие нормативных документов (50,0%) и связанная с этим недостаточная подготовка специалистов ультразвуковой диагностики по вопросам обеспечения эпидемиологической безопасности (27,8%). Справедливости ради необходимо отметить, что опрос 1029 специалистов ультразвуковой диагностики из 60 стран со всех континентов мира, проведенный WFUMB в 2016 г., результаты которого представлены в работах S.C. Westerway и соавт. [26, 27], также показал серьезные пробелы в знаниях основных мер профилактики инфекций, ассоциированных с проведением УЗИ. Это послужило толчком к разработке расширенных международных и национальных рекомендаций [17–23].
Обсуждение
Полученные результаты наглядно свидетельствуют о наличии потенциальных рисков трансмиссии возбудителей инфекционных болезней (патогенных и условно-патогенных бактерий, грибов и некоторых вирусов) между пациентами при проведении всех видов УЗИ. К сожалению, в РФ не принята международная классификация медицинских изделий на некритические, полукритические и критические по риску их использования для пациента (низкий, средний и высокий соответственно). Классификация медицинских изделий Сполдинга [28] проста и понятна. Она позволяет привести в соответствие порядок обработки медицинского изделия перед повторным использованием с инфекционными рисками, которые оно несет. Например, чрескожный датчик, используемый на интактной коже у здорового пациента без покрытия, контаминируется резидентной и транзиторной микрофлорой кожи пациента. Инфекционные риски в данном случае низкие, поэтому после завершения исследования датчик необходимо очистить и подвергнуть дезинфекции низкого уровня. Тот же датчик на интактной коже пациента с инфекцией, передающейся контактным путем, контаминируется не только резидентной, но патогенной и условно-патогенной микрофлорой, поэтому после исследования он подвергается очистке и дезинфекции среднего уровня. Снизить риски поможет одноразовое нестерильное покрытие. Если же датчик используют на неинтактной коже (рана, мацерация, инфекционный процесс), он имеет прямой контакт с биологическими жидкостями пациента, поэтому риски, связанные с ними, расцениваются уже как средние. После исследования такой датчик необходимо очистить и подвергнуть ДВУ. Опять же снизить уровень риска может одноразовое стерильное покрытие, но оно не заменяет дезинфекцию [18, 23, 29]. Сравнение результатов анкетирования российских специалистов ультразвуковой диагностики, выполняющих чрескожные исследования, и анкетирования, проведенного WFUMB [26], показало сопоставимость результатов. Так, никогда не дезинфицируют чрескожные датчики 38,7% российских и 35,7% зарубежных специалистов. Никогда не используют покрытия при УЗИ пациентов с инфекциями кожи/контактными инфекциями 18,3 и 10,7% специалистов соответственно.
Внутриполостные датчики контактируют со слизистыми оболочками, поэтому по рискам для пациентов относятся к полукритическим изделиям, требующим на финальной стадии обработки ДВУ. Снизить инфекционные риски могут одноразовые стерильные покрытия, но они дополняют дезинфекцию, не заменяя ее. Датчики, проникающие в рану, стерильные ткани по определению должны пройти предстерилизационную очистку, дезинфекцию и стерилизацию. Только невозможность проведения стерилизации из-за конструктивных особенностей датчика, указанная производителем в инструкции по эксплуатации, может служить основанием для замены стерилизации на ДВУ. Использование в этом случае одноразового стерильного покрытия и стерильного проводящего геля в одноразовой расфасовке является обязательным [18, 29]. В соответствии с результатами анкетирования специалистов ультразвуковой диагностики, выполняющих внутриполостные и интервенционные исследования, проведенного WFUMB, никогда не проводят очистку и дезинфекцию внутриполостных датчиков 29,0% респондентов, ДВУ – 8,3% [26]. В нашем исследовании эти показатели составили 16,8 и 63,7% (с учетом применения неэффективных средств ДВУ – 83,9%) соответственно. Причина низкого охвата ДВУ датчиков понятна. Она заключается в том, что эта дезинфектологическая технология в нашей стране законодательно распространяется исключительно на гибкие эндоскопы. Вероятно, в качестве компенсаторной меры российские специалисты используют одноразовые покрытия для этого вида датчиков в 97,0% случаев, однако только 65,7% из них относится к стерильным.
Проведенное анкетирование не охватило всех аспектов профилактики инфекций, связанных с проведением УЗИ. Мы не рассмотрели вопросы, возникающие при использовании геля, выполнении специалистами правил личной гигиены, проведении профилактической дезинфекции. Однако полученные и проанализированные материалы помогли установить несколько важных причин, которые не позволяют гарантировать эпидемиологическую безопасность ультразвуковой диагностики. Прежде всего, это отсутствие нормативных документов. Использование зарубежных рекомендаций профильных ассоциаций и производителей датчиков затруднено, так как рекомендуемая ими ДВУ для внутриполостных и интервенционных датчиков и методы ее выполнения российскими санитарно-эпидемиологическими правилами не нормированы. Для выполнения ДВУ в нашей стране регламентирован исключительно способ погружения изделия в раствор стерилизующего средства на время, установленное инструкцией на это средство, с последующими ополаскиванием и сушкой. Как подтвердило исследование, корректное выполнение ДВУ в условиях потока пациентов невозможно. Способы протирания системой спороцидных салфеток, использование установок, зарегистрированных для ДВУ датчиков, в нашей стране не нормированы. Кроме того, выбор дезинфицирующего средства, а также режима и способа его применения в зависимости от области выполняемого УЗИ требует нормирования и специальных знаний у специалистов ультразвуковой диагностики.
Отсутствие простых и понятных стандартов обработки датчиков заставляет врача искать собственные варианты. Множество используемых алгоритмов обработки чрескожных, внутриполостных и интраоперационных датчиков свидетельствует о серьезности этой проблемы.
Недостатком работы является высокая вероятность ответов на вопросы наиболее заинтересованной и компетентной частью медицинского сообщества, поскольку анкета была разослана 7000 врачей ультразвуковой диагностики, а ответы получены только от 869 (12,4%) из них. Возможно, в реальности ситуация менее благоприятна по сравнению с представленной в статье. Но это еще раз доказывает необходимость скорейшего нормирования требований эпидемиологической безопасности.
Заключение
Анализ материалов опроса специалистов ультразвуковой диагностики позволил выявить потенциальные риски инфицирования пациентов:
1) отсутствие дезинфекции чрескожных и внутриполостных датчиков между пациентами в 38,7 и 16,8% случаев соответственно;
2) проведение на финальной стадии обработки интраоперационных датчиков только дезинфекции в 50,0% случаев;
3) применение дезинфицирующих средств и способов, которые не могут обеспечить эффективность обработки, в 65,6% случаев при внутриполостных УЗИ;
4) использование нестерильных покрытий на внутриполостные датчики в 34,3% случаев;
5) нерегулярное использование стерильных одноразовых покрытий в 9,3% случаев при интраоперационных УЗИ;
6) недостаточные знания специалистов ультразвуковой диагностики в вопросах обеспечения эпидемиологической безопасности проводимых ими исследований и защиты собственного здоровья;
7) отсутствие обоснованных и разработанных национальных рекомендаций по обеспечению эпидемиологической безопасности ультразвуковой диагностики.
Проведенное исследование подтвердило актуальность проблемы обеспечения эпидемиологической безопасности ультразвуковой диагностики и необходимость создания системы эпидемиологической безопасности с нормированием требований к ее основным компонентам. Эти требования могут войти в санитарно-эпидемиологические правила или совместные клинические рекомендации РАСУДМ и Национальной ассоциации специалистов по контролю инфекций (НАСКИ).



