Известно, что новая коронавирусная инфекция COVID-19 приводит к сохраняющимся изменениям, которые принято обозначать как постковидный синдром [1]. Важным его проявлением являются тромботические осложнения, совокупная частота которых достигает 3,19% [2]. В ряде зарубежных исследований показано, что микротромбоз является причиной «мозгового тумана» [3, 4], телогенной алопеции и некоторых других сердечно-сосудистых, легочных, ольфакторных проявлений [5]. В то же время продолжительность гиперкоагуляции у перенесших COVID-19 пациентов до сих пор не установлена, так как диагностика протромботического состояния связана со значительными трудностями. Известно, что отклонения в классическом биохимическом тесте коагулограммы и уровне D-димера в реконвалесцентном периоде COVID-19 встречаются редко. А значение глобальных тестов оценки гемостаза (активно применяющихся в остром периоде COVID-19 [6]) не изучено. С другой стороны, есть исследования, убедительно демонстрирующие одинаковую частоту тромбозов и кровотечений после выписки из стационара по поводу COVID-19 и вообще отсутствие увеличения риска тромботических событий в постковидном периоде [7, 8]. Поэтому показания к тромбопрофилактике после окончания стационарного лечения в настоящее время спорны, что отражается в противоречивых рекомендациях экспертов.
Цель работы – оптимизация диагностики и терапии нарушений гемостаза в постковидном периоде. Для достижения цели были поставлены задачи изучить клинико-лабораторные признаки нарушений гемостаза у больных в постковидном периоде; определить значение глобального теста оценки гемостаза в этом периоде; провести медикаментозную коррекцию патологии гемостаза у реконвалесцентов COVID-19 и обосновать выбор терапевтических режимов.
Материалы и методы
Работа проведена во ФГБОУ ВО «Кубанский государственный медицинский университет» Минздрава России на базе дневного стационара ГБУЗ «Специализированная клиническая инфекционная больница» (СКИБ) Министерства здравоохранения Краснодарского края с апреля 2021 г. по декабрь 2022 г. Были обследованы 100 пациентов молодого и среднего возраста (М = 50,5 ± 0,84 года), перенесших среднетяжелое (n = 55), тяжелое и крайне тяжелое (n = 45) течение COVID-19. Контрольную группу, обследованную амбулаторно, составили 20 условно здоровых лиц (М = 45 ± 1,6 года), не переносивших коронавирусную инфекцию (клинически и серологически) и не вакцинированных от COVID–19. Исследование проведено в дизайне одноцентрового когортного ретроспективно-проспективного сравнительного нерандомизированного.
Критерии включения: возраст от 18 до 60 лет, добровольное информированное согласие на участие в исследовании, подтвержденный диагноз COVID-19 во время госпитализации в ковидный госпиталь СКИБ за 6 мес. до настоящего исследования в условиях дневного стационара (первый этап).
На этом этапе всем пациентам выполнены общепринятые клинические и лабораторные исследования (ОАК, ОАМ, копрограмма, расширенный биохимический анализ крови); определение уровней С-реактивного белка, ревматоидного фактора, магния, холинэстеразы, ферритина, гликозилированного гемоглобина, 25-ОН витамина D, тропонина I, NT-proBNP, ТТГ, пролактина, тестостерона, прогестерона, АТ-ТПО, ANA, AMA, ANCA; иммунограмма; ИФА на антитела IgM и IgG к SARS-CoV-2; компьютерная томография (КТ) органов грудной клетки, эхокардиография и спирометрия. Состояние системы гемостаза оценивали по уровню тромбоцитов и тромбоцитарным индексам (анализатор Beckman Coulter LH 500, США): показателям активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени (ПТВ), международного нормализованного отношения (МНО), тромбинового времени (ТВ), фибриногена, AТ-III, D-димера (на автоматическом коагулометре Sysmex CS-2100i/CS-2000i фирмы Siemens, Германия). Диагностику ковид-ассоциированной коагулопатии проводили в соответствии с критериями, предложенными экспертами Международного общества по тромбозам и гемостазу [9].
Всем пациентам выполнен тест тромбодинамики (ТД) с помощью лабораторной диагностической системы «Регистратор тромбодинамики Т-2» (ООО «ГемаКор», Россия) с определением задержки роста сгустка (Tlag), скорости роста сгустка (V), стационарной скорости роста сгустка (Vst), размера сгустка через 30 мин. (СS), плотности сгустка (D), начальной скорости роста сгустка (Vi) и времени появления спонтанных сгустков (Tsp). Состояние выраженной гиперкоагуляции констатировали при V > 30 мкм/мин и спонтанном образовании сгустков и/или при V > 40 мкм/мин без спонтанного образования сгустков; умеренной гиперкоагуляции – при V > 30 мкм/мин и отсутствии спонтанного образования сгустков, нормокоагуляции – при V = 20–29 мкм/мин и Tlag < 0,5 мин.
В зависимости от результатов ТД на втором этапе все пациенты были разделены на 3 группы, которым предложен разный алгоритм коррекции нарушений гемостаза. Пациентам группы А (n = 35) с преимущественной выраженной гиперкоагуляцией были предложены прямые оральные антикоагулянты (ПОАК) ривароксабан 10 мг в сутки или апиксабан 5 мг в сутки в течение 12 нед. Пациентам группы В (n = 45) с преимущественной умеренной гиперкоагуляцией назначен сулодексид по 250 ЛЕ 2 раза в сутки в течение 12 нед. В группу С (n = 20) вошли больные с различными невыраженными расстройствами гемостаза или не приверженные назначенной медикаментозной терапии, которые не принимали лекарственные средства, влияющие на гемостаз, в течение 12 нед. Через 3 мес. (12 нед.) или всего 9 мес. после выписки из ковидного госпиталя СКИБ всем пациентам проводили контрольный тест ТД (валидационный этап исследования). Исследование одобрено локальным этическим комитетом.
Полученный материал обрабатывали методом вариационной статистики с использованием электронных таблиц Microsoft Excel из пакета программ Microsoft Office 2019 и при помощи программного обеспечения Statistica version 10 (StatSoft Inc., США). Результаты представлены в виде абсолютных значений, доли от общего, среднего и его стандартного отклонения (M ± SD) – при нормальном распределении признака, медианы (Me) и интерквартильного размаха (Q1–Q3) – при ненормальном распределении. Нормальность распределения переменных проверяли с помощью теста Колмогорова–Смирнова. Для сравнения выборок с категориальными переменными использовали анализ таблиц сопряженности. Из таблицы сопряжения также рассчитывали отношение шансов (OШ) с 95% доверительным интервалом [95% ДИ]. Для сравнения независимой переменной более чем в двух выборках выполнен многофакторный дисперсионный анализ ANOVA с расчетом критерия Краскела–Уоллиса. При значении р < 0,05 отличия считали статистически значимыми. Для оценки взаимосвязей между непрерывными переменными определен коэффициент прямой линейной корреляции Спирмена (r). Взаимосвязь между параметрами считалась очень высокой, если r лежал в диапазоне 0,9 и выше, тесной – при 0,7–0,89, значительной – при 0,51–0,69, умеренной – при 0,5–0,31, слабой – при 0,3–0,11.
Результаты
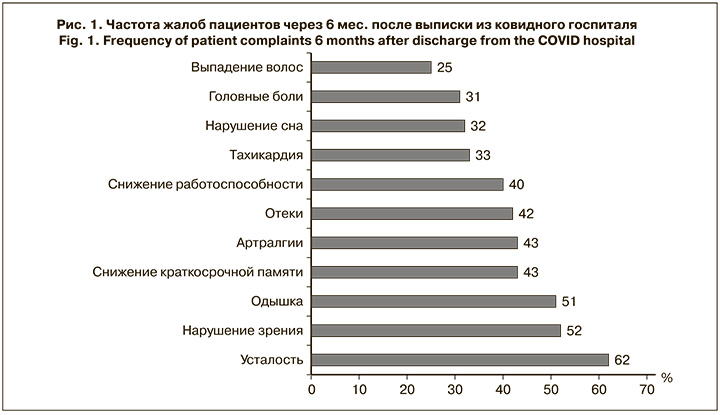
В исследовании приняли участие 51 женщина и 49 мужчин. Среди фоновых заболеваний наиболее часто встречались гипертоническая болезнь (42%), ожирение 1–3-й степени (35%), сахарный диабет (20%), хронический панкреатит (19%). Через 6 мес. после выписки из ковидного госпиталя СКИБ пациенты предъявляли множество жалоб, наиболее частые представлены на рис. 1. Необходимо отметить, что в течение этого периода клинических признаков тромботических событий и/или кровотечений не зарегистрировано ни у одного больного. Средний уровень тромбоцитов составил 258,26 ± 5,77 × 109/л. Тромбоцитопения < 150 × 109/л зарегистрирована только у 2 пациентов. MPV – 10,64 ± 0,08 фл, что статистически значимо превышало верхнюю границу интервала. При этом ни уровень тромбоцитов, ни MPV не зависели от тяжести перенесенной COVID-19.
В целом для постковидного периода изменения биохимической коагулограммы не были характерны. АЧТВ составило 32,2 ± 0,47 с, ПТВ – 11,85 ± 0,08 с, МНО – 0,96 ± 0,01, уровень фибриногена – 3,46 ± 0,08 г/л. МНО > 1,2 не зарегистрировано ни в одном случае. Гиперфибриногенемия > 4 г/л отмечена у 23 (23%) пациентов. Самым частым изменением клоттинговых тестов было незначительное удлинение ТВ – 21,49 ± 0,1 с в сочетании с неизмененными АЧТВ и ПТВ, так же, как и в остром периоде. Уровень D-димера составил 0,36 ± 0,02 мкг/мл, тогда как в остром периоде максимальный показатель был в 10,8 раза выше – 3,9 ± 0,31 мкг/мл. Повышение уровня D-димера > 1,1 мкг/ мл, необходимое для диагностики ковид-ассоциированной коагулопатии, не зарегистрировано в постковидном периоде ни в одном случае.
По данным теста ТД, V составила в среднем 35,43 ± 0,75 мкм/мин, что значительно превышало показатели группы контроля (27,81 ± 0,84 мкм/мин); а Tlag, D, CS от контрольных значений не отличались. У 31 пациента наблюдали появление спонтанных сгустков. Выраженная гиперкоагуляция зарегистрирована у 39 (39%) чел., умеренная гиперкоагуляция – у 47 (47%), нормокоагуляция – у 14 (14%), гипокоагуляции не выявлено. Формирование гиперкоагуляционного состояния (86%) не зависело от тяжести перенесенного острого заболевания (OШ = 0,51; 95% ДИ 0,17–1,59). В контрольной группе выраженная гиперкоагуляция не встречалась, умеренная гиперкоагуляция отмечена у 29% пациентов, нормокоагуляция – у 71%. Установлена статистическая значимость долевых различий (р < 0,05).
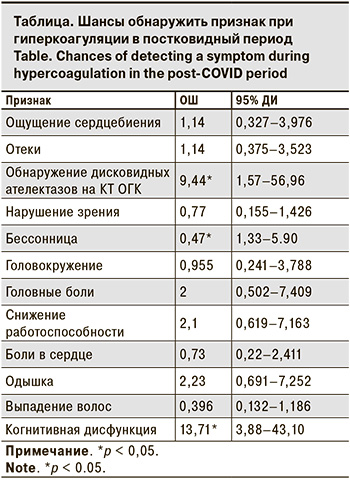
Взаимосвязь гиперкоагуляции с клиническими проявлениями постковидного периода представлена в таблице. Статистически значимую связь установили между гиперкоагуляцией и когнитивной дисфункцией (ОШ = 13,71; 95% ДИ 3,88–43,10), между гиперкоагуляцией и обнаружением дисковидных ателектазов на КТ органов грудной клетки (ОГК) (ОШ = 9,44; 95% ДИ 3,88–43,10). А вот бессонницу при гиперкоагуляции регистрировали достоверно реже.
Кроме того, у пациентов с гиперкоагуляцией выявлен достоверно более высокий уровень СРБ, чем у пациентов с нормокоагуляцией (3,94 и 3,48 мг/л соответственно); статистически значимо меньшее содержание альбумина в крови (47,6 и 49,9 г/л; р = 0,01); был достоверно повышен компонент С4 комплемента (35,8 и 34,6) и антитела к ТПО (329,56 и 31,78 МЕ/мл). Установлены более высокий уровень гликогемоглобина и низкий уровень магния в крови у всех пациентов с постковидным синдромом по сравнению с контрольной группой. Более высокая статистически значимая V обнаружена у пациентов с хроническим панкреатитом – 37,45 (31,375–40,825) мкм/мин, чем у пациентов без фоновой патологии поджелудочной железы – 34,6 (31,6–40,1) мкм/мин. В постковидном периоде у больных с ожирением оказались значимо более высокими показатели фибриногена – 3,6 г/л (3–4,1), СРБ – 3,9 мг/л (2,8–6,2), ферритина – 149,7 мкг/л (71,86–273), чем у пациентов без ожирения: 3,35 г/л (2,9–3,825), 2,65 мг/л (1,2–3,6), 86,5 мкг/л (50,4–164,1) соответственно. У пациентов с гипертонической болезнью и сахарным диабетом достоверной разницы в значениях показателей гемостаза не выявлено.
При изучении связи показателей биохимической коагулограммы и ТД в постковидный период (рис. 2, см. на вклейке) установлена умеренная положительная статистически значимая корреляция между показателем D теста ТД и МНО (r = 0,34; p = 0,016); умеренная (ближе к значительной) – между фибриногеном и D (r = 0,5; p = 0,0007); умеренная, но недостоверная – между V и D-димером (r = 0,37; p = 0,08); умеренная отрицательная – между V и АЧТВ (r = -0,37; p = 0,008).
У пациентов группы А (n = 35) после 12-недельного приема ПОАК V существенно уменьшилась (с 40,6 ± 1,9 до 31,5 ± 1,5 мкм/мин), разница была статистически значимой (рис. 3, а, см. на вклейке). Также достоверно увеличилось Tsp (с 20,2 ± 1 до 26,2 ± 1,5 мин.) (рис. 3, в, см. на вклейке) и снизилась Vi (с 51,5 ± 1 до 50,9 ± 1,2 мкм/мин) (рис. 3, с, см. на вклейке). Через 30 мин. СS и D статистически значимо не изменялись. В целом доля пациентов с выраженной гиперкоагуляцией (73%) уменьшилась больше чем в 2 раза (с 73 до 35%), а у 41% исследуемых констатирована нормокоагуляция.
Полученные данные показывают явное положительное влияние на гиперкоагуляционное состояние, отражают хорошую эффективность ПОАК. За 12 нед. применения ривароксабана или апиксабана геморрагических осложнений не было зарегистрировано ни у одного пациента.
У пациентов группы В (n = 45) отмечено уменьшение V с 36,2 ± 1,3 до 33,7 ± 1,4 мкм/мин (рис. 3, d, см. на вклейке), но различия не были статистически значимыми (p = 0,36). Уменьшался CS через 30 мин.: до коррекции – 1239 мкм (1159–1364), после – 1183 мкм (1111–1238) и после приема сулодексида уже не отличался от CS в контрольной группе (рис. 3, e). К сожалению, появление спонтанных сгустков продолжалось и по времени не отличалось от показателя Tsp до коррекции (рис. 3, f, см. на вклейке). Показатели Tlag, Vst и D существенно не различались. Действие препарата привело к появлению нормокоагуляции лишь в 16% случаев, что отражает его умеренную эффективность. Применение сулодексида было безопасным, нежелательных явлений не зарегистрировано.
В группе С (без медикаментозной коррекции; n = 20) через 9 мес. после выписки из стационара V оставалась достоверно повышенной по сравнению с контролем: 33,5 мкм/мин (30,6–39,4) и 27,4 мкм/мин (25–29,3) соответственно и не отличалась от показателя через 6 мес. – 34,3 мкм/мин (30,9–40) (рис. 3, g, см. на вклейке). Также значительно и статистически значимо (р < 0,05) отличалось от показателей контрольной группы Tsp (рис. 3, h, см. на вклейке), что говорит о продолжающемся процессе образования спонтанных сгустков и через 9 мес. постковидного периода при условии отсутствия медикаментозной коррекции. Только показатель Tlag со временем достоверно не отличался от контроля (рис. 3, i, см. на вклейке). Таким образом, и через 9 мес. постковидного периода у половины пациентов сохраняется гиперкоагуляционное состояние, что статистически значимо чаще, чем в контрольной группе.
Обсуждение
Полученные данные показывают, что постковидный период сопряжен не только с общепризнанными проявлениями (астено-вегетативными, респираторными, нервно-психическими, сердечно-сосудистыми), частота встречаемости которых в нашем исследовании не отличалась от данных, приведенных в зарубежных и отечественных публикациях [4, 5, 10, 11], но и с патологией системы гемостаза. Мы установили, что через 6 мес. после выписки из стационара у 86% пациентов отмечается высокий протромботический потенциал плазмы, о чем свидетельствуют образование спонтанных сгустков (Tsp), ускорение роста сгустка при ТД. К гиперкоагуляции может приводить присутствие в крови активированных факторов свертывания, тканевого фактора, повышенная концентрация прокоагулянтных микровезикул [12]. Показано, что микротромбоз связан с проявлениями когнитивной дисфункции со снижением памяти, концентрации внимания и «мозговым туманом»; образованием дисковидных ателектазов в легких; панкреатодисфункцией. Установлено также, что гиперкоагуляция в постковидном периоде лишь отчасти зависела от коморбидных состояний. Наибольшее влияние на систему гемостаза в периоде реконвалесценции оказывало ожирение за счет возможной пролонгации воспалительного процесса и связанной с ним эндотелиопатии. А природа панкреатодисфункции и ее сочетание с гиперкоагуляцией нуждаются в дальнейшем изучении. Отсутствие же явных тяжелых тромботических событий в течение 6-месячного постковидного периода у наших пациентов могло быть связано со включением в исследование только людей молодого и среднего возраста, а также отражало недостаточный целенаправленный поиск венозных тромбоэмболий (не были выполнены ультразвуковая допплерография сосудов нижних конечностей и КТ-ангиография легких). В целом мы согласны с исследователями, не считающими тяжелые тромботические события частыми проявлениями постковидного периода [13].
Скромные клинические проявления вовсе не означают отсутствия лабораторных изменений. Так, увеличение среднего объема тромбоцитов в ОАК свидетельствует об адекватной стимуляции выброса костным мозгом тромбоцитарных элементов. Характерным изменением коагулограммы в постковидном периоде было увеличение ТВ с неизмененными АЧТВ и ПТВ, что отражает процесс нарушения полимеризации фибрина и образования большого количества продуктов его деградации. Гиперфибриногенемия, зарегистрированная почти у четверти пациентов через 6 мес. реконвалесцентного периода, может приводить к нарушению микроциркуляции и выработке аутоантител [14, 15]. А корреляция фибриногена с показателем плотности сгустка (D) ТД свидетельствует о пропорциональной плотности фибриновой сети. В целом изменения биохимической коагулограммы и уровня D-димера в постковидном периоде были невыраженными. А вот на основании исследования гемостаза с помощью простого в исполнении и информативного глобального теста – ТД получены доказательства сохраняющегося гиперкоагуляционного состояния у реконвалесцентов COVID-19 вплоть до 9 мес. постковидного периода. Наиболее выраженные изменения наблюдали в первые 6 мес. у 86% пациентов, они не зависели от тяжести перенесенного острого заболевания. Установленные нами корреляционные связи (фибриноген и плотность сгустка, АЧТВ и скорость роста сгустка, скорость роста сгустка и D-димер) говорят о равнонаправленном векторе изменений ТД и биохимической коагулограммы, однако ТД оказался значимо более чувствительным методом диагностики.
В результате дифференцированной коррекции нарушений гемостаза определено, что нормализующее действие на систему гемостаза оказывал длительный (не менее 3 мес.) прием ПОАК в профилактической дозировке. Такой режим коррекции эффективен, безопасен и является оптимальной терапевтической опцией для пациентов с выраженной гиперкоагуляцией. Применение сулодексида, на первый взгляд, было не столь эффективно. Однако уменьшение СS до размеров, сопоставимых с показателями в контрольной группе, означает мягкое нормализующее действие препарата, так как СS – это интегральная характеристика, которая отражает совокупную работу всех элементов свертывающей системы. Так как через 9 мес. постковидного периода у половины пациентов без медикаментозной коррекции сохранялось гиперкоагуляционное состояние, можно заключить, что спонтанной нормализации гемостаза в эти сроки еще не происходит.
Заключение
Полученные нами результаты позволяют расширить существующие данные о диагностике, клинических проявлениях и терапии нарушений в системе гемостаза в постковидный период. На основании исследования гемостаза с помощью простого в исполнении и информативного глобального теста – ТД получены доказательства сохраняющегося гиперкоагуляционного состояния у реконвалесцентов COVID-19 вплоть до 9 мес. постковидного периода. Наиболее выраженные изменения наблюдались в первые 6 мес. и не зависели от тяжести перенесенного острого заболевания. При выраженной гиперкоагуляции эффективно и безопасно применение профилактических доз ПОАК в течение 12 нед. Сулодексид уместно использовать при умеренной гиперкоагуляции. Эти данные отличаются от существующих на сегодняшний день алгоритмов профилактики отдаленных тромботических осложнений1 [16].



