Проблема туберкулеза с множественной лекарственной устойчивостью (МЛУ ТБ) возбудителя в последние годы стоит особенно остро. Несмотря на то что продолжается мировая тенденция к снижению как заболеваемости, так и смертности от ТБ, темпы улучшения показателей сдерживает тот факт, что значительная их часть формируется статистикой по случаям с МЛУ ТБ. Большое значение имеет низкая эффективность лечения МЛУ ТБ по сравнению с ТБ с сохраненной лекарственной чувствительностью возбудителя. По данным ВОЗ, за прошедшее десятилетие число случаев МЛУ ТБ в мире возросло почти вдвое. Ежегодно лекарственная устойчивость возбудителя к рифампицину развивается более чем у полумиллиона человек, из них 78% имеют подтвержденный МЛУ ТБ. Успешное лечение МЛУ ТБ наблюдается лишь в 57% случаев [1]. Из-за длительности курса лечения (9–20 мес.) и частых случаев неуспешного лечения национальные органы здравоохранения несут значительные расходы. Так, по результатам систематического обзора Y.V. Laurence и соавт. [2], затраты на лечение 1 пациента с МЛУ ТБ составляют 1218–83 365 долларов США (в зависимости от уровня дохода страны), что примерно в 5 раз превышает затраты на лечение ТБ с сохраненной лекарственной чувствительностью возбудителя.
Российская Федерация входит в список 20 стран, вносящих наибольший вклад в мировое абсолютное число инцидентных случаев МЛУ ТБ (согласно математическим оценкам бремени ТБ ВОЗ). Азербайджанская Республика, Республика Беларусь, Киргизская Республика и Республика Таджикистан входят в число 10 стран с наивысшей заболеваемостью МЛУ ТБ в пересчете на численность населения страны; Республика Армения исключена из этого списка лишь с 2016 г. [3].
Другой глобальной угрозой, препятствующей радикальному снижению показателей заболеваемости и смертности, и, как следствие, расходов на лечение ТБ, является ВИЧ-инфекция [1]. Результаты последних исследований подтверждают, что она является одним из неблагоприятных факторов, повышающих вероятность развития МЛУ ТБ, поэтому программы ускоренного тестирования, рекомендованные ВОЗ, а также другие меры, направленные на повышение показателей успеха лечения и снижение дальнейшего распространения МЛУ ТБ, особенно важны для людей, живущих с ВИЧ [4].
В настоящее время в отношении всех случаев рифампицин-резистентного ТБ (РР ТБ), включая случаи МЛУ ТБ, рекомендуется единая стратегия терапии [5]. Высокий охват тестированием на ТБ молекулярно-генетическими методами (включающая определение устойчивости возбудителя к рифампицину) не только уменьшает резервуар невыявленных случаев заболевания, но и позволяет в кратчайшие сроки выбрать верную стратегию лечения, что положительно сказывается на показателях успешного лечения МЛУ ТБ.
Цель исследования – изучение динамики показателей охвата тестированием, распространенности и успеха лечения МЛУ ТБ среди больных ВИЧ-инфекцией в странах СНГ за период 2010–2018 гг.
Материалы и методы
Исследование проведено в рамках проекта: «Комплексный анализ медико-биологических и социально-демографических факторов риска развития туберкулеза у пациентов с ВИЧ-инфекцией». Для выполнения целей исследовательской работы в 2019 г. был проведен сбор эпидемиологических данных в Азербайджанской Республике, Республиках Армения, Беларусь, Киргизской Республике, Республике Таджикистан и в одном из субъектов Центрального федерального округа РФ – Владимирской области. Выбор Владимирской области был определен тем, что регион имеет средние по стране показатели пораженности ТБ и ВИЧ-инфекцией. Кроме того, в регионе действует единая лаборатория для выявления и идентификации микобактерий, которая регулярно участвует в Федеральной системе внешней оценки качества клинических лабораторных исследований (ФС ВОК).
В качестве инструмента сбора данных была использована стандартизированная форма, в заполнении которой приняли участие представители представителей противотуберкулезных служб стран-участниц проекта, а также Республиканских центров СПИД. Источниками эпидемиологических данных служили национальные базы учета случаев заболевания, государственные регистры данных, материалы ведомственной статистической отчетности, данные фтизиатрических служб и государственных статистических служб, а также материалы регулярной отчетности стран в ВОЗ и UNAIDS.
Результаты
С 2010 по 2018 г. число инцидентных1 случаев с подтвержденным МЛУ ТБ в странах-участницах исследования изменялось неравномерно. В Азербайджане, Киргизии и Таджикистане показатели в изучаемый период выросли и достигли максимального значения в 2018 г. (рис. 1, см. на вклейке). При этом в Киргизской Республике показатель стабильно рос, в Азербайджанской Республике динамика изменения показателя имела скачкообразный характер, в Республике Таджикистан линия роста была неравномерной с пиком в 2014 г. Наибольший ежегодный прирост был зарегистрирован в Республике Таджикистан (39,6%) и Киргизской Республике (23,6%).
В Республиках Беларусь и Армения, а также во Владимирской области значение показателя несколько снизилось. Так, средняя годовая убыль за изучаемый период во Владимирской области составила 8%, в Республике Беларусь – 7,3%, в Республике Армения – 3,5%. При этом во Владимирской области снижение числа случаев происходило равномерно, но в других странах зарегистрирован кратковременный рост: в 2015 г. в Беларуси и в 2016 г. в Армении. На рис. 2 (см. на вклейке), где показатели Владимирской области и Республики Армения вынесены на дополнительную ось ординат, хорошо прослеживается тенденция снижения показателя в 2017–2018 гг. во всех трех территориях.
Вместе с тем число случаев МЛУ ТБ, зарегистрированных среди всех категорий пациентов (включая не только впервые выявленных и рецидивы, но и другие категории) в изучаемый период не снизилось в 5 странах из числа принявших участие в исследовании (рис. 3, см. на вклейке). Совокупная оценка динамики числа всех зарегистрированных случаев показывает прирост показателя с 2010 по 2018 г., при этом интенсивность и объем прироста варьировали. Наибольший средний годовой прирост отмечен в Киргизской Республике (24,2%) и Республике Таджикистан (16,6%); небольшое увеличение показателей зафиксировано в Республиках Армения (средний годовой прирост составил 2,4%), Беларусь (6,5%) и в Азербайджанской Республике (8,4%).
В ходе исследования охват инцидентных случаев ТБ тестированием на лекарственную чувствительность (ТЛЧ) постепенно повышался в Азербайджанской и Киргизской Республиках, Республике Таджикистан (рис. 4, см. на вклейке). Следует отметить, что прирост показателя был значительно меньше, чем рост абсолютного числа случаев МЛУ ТБ. Так, в Киргизской Республике, где интенсивно увеличивается число случаев МЛУ ТБ (средний ежегодный прирост в 2010–2018 гг. составил 24,2%, в 2016–2018 гг. среднегодовой прирост числа диагнозов МЛУ ТБ среди инцидентных случаев – 9,5%), средний ежегодный прирост охвата пациентов ТЛЧ составил 9%; в 2016–2018 гг. охват тестированием инцидентных случаев ТБ увеличивался в среднем всего на 1,5% в год. В Республике Таджикистан на фоне стремительного роста абсолютного числа инцидентных случаев МЛУ ТБ (средний ежегодный прирост – 39,6%) средний ежегодный прирост показателя охвата инцидентных случаев тестированием составил 12%.
В Республике Беларусь и Владимирской области в течение исследуемого периода ТЛЧ выполняли для всех инцидентных случаев ТБ.
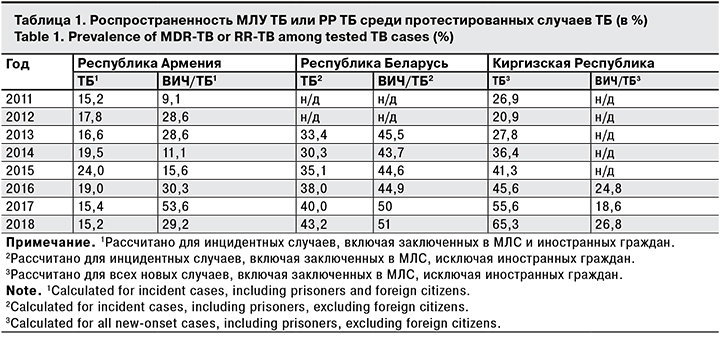
На основании собранных в рамках исследования данных можно предположить, что выявляемость РР ТБ среди ВИЧ-положительных пациентов была выше, чем среди когорты протестированных больных ТБ без подтвержденной ВИЧ-инфекции в большинстве стран, в которых имелись данные по этим показателям. Исключение составила Киргизская Республика, где обратная картина может быть связана с низким охватом ТЛЧ (табл. 1). При этом средний ежегодный прирост доли пациентов с МЛУ ТБ среди пациентов с ВИЧ-инфекцией за исследуемый период в Республике Армения составил 46%, в Киргизской Республике – 10%, в Республике Беларусь – 2,4%.
В странах, принявших участие в исследовании, наименьшие значения показателей успеха лечения зафиксированы для подгрупп пациентов ВИЧ/МЛУ ТБ. Так, в 2016 г. во всех странах, предоставивших данные об успешном лечении новых случаев лекарственно чувствительного (ЛЧ ТБ), МЛУ или РР ТБ у больных ВИЧ-инфекцией значения показателя успеха лечения значительно различались: в Республике Армения доля успешно пролеченных ЛЖВ с ЛЧ ТБ была в 3,4 раза выше, по сравнению с больными ВИЧ-инфекцией и МЛУ или РР ТБ, в Республике Беларусь – в 2 раза, в Киргизской Республике – в 1,4 раза, в Республике Таджикистан – в 1,9 раза, во Владимирской области РФ – в 1,4 раза. В динамике с 2011 по 2016 г. не было отмечено устойчивой тенденции по показателю успеха лечения МЛУ/РР ТБ у ВИЧ-инфицированных пациентов, его значения существенно колебались в Республиках Армения, Таджикистан и Киргизской Республике. В Республике Беларусь с 2014 г. и во Владимирской области с 2013 г. растет доля успешно пролеченных ВИЧ-положительных пациентов с МЛУ ТБ или РР ТБ (табл. 2).

Обсуждение
Единой тенденции в динамике показателей МЛУ ТБ у больных ВИЧ-инфекцией в исследуемых регионах не наблюдалось. Пик заболеваемости на различных территориях приходился на разные годы, в части стран зарегистрировано некоторое снижение числа инцидентных случаев МЛУ ТБ, однако совокупная оценка числа всех учтенных случаев свидетельствовала о росте численности больных МЛУ ТБ. Темпы прироста варьировали, наименьший среднегодовой прирост отмечен в Республиках Армения и Беларусь.
В период с 2010 по 2018 г. постепенно увеличивался охват населения ТЛЧ ТБ, однако не было выявлено четкой корреляции между приростом охвата и увеличением абсолютного числа случаев МЛУ ТБ. Сравнение в когортах ВИЧ/ТБ и всех случаев ТБ показало, что РР ТБ в первой когорте выявляется чаще, что может быть связано как с более высокой частотой РР ТБ среди ВИЧ-инфицированных (что согласуется с данными других авторов), так и с более высокой частотой бактериологически подтвержденного ТБ в когорте больных ВИЧ/ТБ в части стран, принявших участие в исследовании [4].
Показатели успеха лечения МЛУ ТБ у больных ВИЧ/ТБ по-прежнему значительно отстают от таковых при ЛЧ ТБ, и существенной динамики за период наблюдения достигнуто не было. По свидетельству ВОЗ, худшие результаты лечения среди больных ВИЧ-инфекцией объясняются несвоевременной диагностикой ТБ, ассоциированного с ВИЧ, и, как следствие, поздним началом противотуберкулезной и антиретровирусной терапии [6].
Заключение
Особенности национальных систем учета и организации сбора эпидемиологических показателей по ТБ и ВИЧ-инфекции не позволяют получить однородный массив данных для анализа по всем запрошенным параметрам. Так, в Республике Киргизия данные о доле ВИЧ-положительных пациентов с МЛУ ТБ регистрируются с 2016 г.; частично отсутствуют данные о доле успешно пролеченного МЛУ ТБ у пациентов с ВИЧ-инфекцией в Республиках Беларусь, Таджикистан и Киргизской Республике. Однако имеющиеся данные позволяют проследить тенденции в распространении МЛУ ТБ у пациентов с ВИЧ-инфекцией в странах СНГ.
Данные о резервуарах МЛУ ТБ в регионах с высоким уровнем миграции могут быть использованы для прогнозирования эпидемической ситуации, а также для расчета ресурсов на программы по борьбе с МЛУ ТБ.



