Крымская геморрагическая лихорадка (КГЛ) – особо опасная природно-очаговая трансмиссивная арбовирусная инфекция. Заболевание встречается в странах Восточной, Западной и Южной Африки, Китае, Афганистане, Иране, Ираке, Индии, Египте, Сирии, ОАЭ, Молдавии, Болгарии, Венгрии, Греции, Югославии, Франции, Испании и ограничено 50° северной широты географического распространения клещей рода Hyalomma [1].
На территории стран СНГ КГЛ распространена на юге Европейской части России, где c 2009 по 2018 г. диагностировано 980 случаев заболевания (2,8% летальных исходов) [2], в южных регионах Республики Казахстан (Туркестанской, Жамбыльской и Кызылординской областях), на территории которых с 1948 по 2013 г. заболевание верифицировано у 780 человек. (летальность – 14,8%) [3]. Есть сообщения о случаях КГЛ в других республиках Центральной Азии и на Украине [1, 2].
В соответствии с классификацией патогенных для человека микроорганизмов, вирус КГЛ относится ко II группе патогенности и, согласно принятой ВОЗ классификации патогенности микроорганизмов, к IV группе риска (высокий индивидуальный и общественный риск)1. Это единственная геморрагическая лихорадка на территории СНГ, входящая в число лихорадок, передача которых может происходить при прямых контактах с пациентом.
Особую опасность представляют тяжелые, прогностически неблагоприятные случаи КГЛ. При оказании медицинской помощи таким больным в значительной степени возрастает риск инфекции, связанной с оказанием медицинской помощи (ИСМП), в лечебно-профилактических учреждениях (ЛПУ) первого и второго уровня (районные и центральные районные больницы), где, как правило, осуществляется лечение пациентов с этим заболеванием [4, 5]. Это нередко связано с отсутствием надлежащего инфекционного контроля в районных стационарах, что обусловлено недостаточной квалификацией медицинского персонала, а также ограниченностью ресурсов и конструктивными недоработками помещений и оборудования. Известен целый ряд случаев инфицирования медицинского персонала КГЛ при уходе за пациентами, связанных с вышеуказанными факторами [6–9].
В связи с этим назрела необходимость разработки клинико-лабораторной балльной шкалы оценки тяжести состояния и риска летального исхода при КГЛ, в соответствии с которой при определенном количестве набранных баллов в день поступления пациента следует незамедлительно переводить в ЛПУ третьего (регионального) уровня, где имеются персонал и ресурсы для оказания высокотехнологичной помощи больным с особо опасными инфекциями, а также в полном объеме осуществляется программа инфекционного контроля, обеспечивающая профилактику ИСМП2.
Из медицинской литературы известна шкала оценки тяжести состояния R. Swanepoel и соавт. [10], согласно которой при наличии определенных сведений в эпидемиологическом анамнезе (контакты с клещами или их присасывание, контакт с биологическими жидкостями пациента с КГЛ, проживание на эндемичной по этому заболеванию территории, контакт с сельскохозяйственными животными на этой территории), клинических проявлений заболевания (лихорадка выше 38 оС, интоксикация, миалгии, различные проявления геморрагического синдрома), а также при определенной выраженности отклонений от нормы лабораторных показателей (анемия, лейкопения, тромбоцитопения, повышение уровня ферментов печени, нарушение показателей свертывающей системы крови) пациента следует вести как больного КГЛ. При максимальной выраженности изменений клинических и лабораторных показателей у пациента есть высокая вероятность летального исхода. Такая методика позволяет проводить дифференциальную диагностику КГЛ с другими заболеваниями со сходной клинической симптоматикой и лабораторными изменениями, а также ориентировочно определять степень тяжести заболевания. Между тем эта шкала не предполагает лабораторной верификации диагноза, что не исключает наличия у пациента другого, отличного от КГЛ заболевания, а также не позволяет оценить риск летального исхода.
 Шкалу оценки тяжести состояния и риска летального исхода при КГЛ разработали также B. Dokuzoguz и соавт. [11]. Она основана на балльной градации выраженности клинических проявлений и изменений показателей гемостаза лабораторно подтвержденного заболевания. Шкала включает клинические проявления заболевания (наличие и выраженность геморрагических симптомов, сонливость), показатели свертывающей системы крови [количество тромбоцитов, уровень фибриногена, АЧТВ (активированное частично тромбопластиновое время)] и позволяет оценивать эффективность различных методов терапии. Эта шкала непосредственно ориентирована на определение степени тяжести, а следовательно и вероятности летального исхода заболевания уже при наличии у пациента подтвержденного диагноза КГЛ. Между тем крайне малый объем анализируемых клинических и лабораторных параметров не позволяет прогнозировать какой-либо исход заболевания с высокой степенью вероятности, что делает ее пригодной лишь для оценки сравнительной эффективности разных схем терапии.
Шкалу оценки тяжести состояния и риска летального исхода при КГЛ разработали также B. Dokuzoguz и соавт. [11]. Она основана на балльной градации выраженности клинических проявлений и изменений показателей гемостаза лабораторно подтвержденного заболевания. Шкала включает клинические проявления заболевания (наличие и выраженность геморрагических симптомов, сонливость), показатели свертывающей системы крови [количество тромбоцитов, уровень фибриногена, АЧТВ (активированное частично тромбопластиновое время)] и позволяет оценивать эффективность различных методов терапии. Эта шкала непосредственно ориентирована на определение степени тяжести, а следовательно и вероятности летального исхода заболевания уже при наличии у пациента подтвержденного диагноза КГЛ. Между тем крайне малый объем анализируемых клинических и лабораторных параметров не позволяет прогнозировать какой-либо исход заболевания с высокой степенью вероятности, что делает ее пригодной лишь для оценки сравнительной эффективности разных схем терапии.
В 2012 г. M. Bakir и соавт. [12] предложили свою шкалу оценки тяжести состояния при КГЛ, основанную на ряде клинических и лабораторных параметров. Модифицированная этими же авторами в 2015 г. шкала позволила прогнозировать неблагоприятный исход заболевания [13]. Она включает возраст пациента, ряд клинических (наличие/отсутствие кровотечений, нарушение функции органов, гепатомегалия) и лабораторных [уровни аспартатаминотрансферазы (АсАт), аланинаминотрансферазы (АлАТ), лактатдегидрогеназы (ЛДГ); количество лейкоцитов и тромбоцитов; показатели гемостаза (АЧТВ), международное нормализованное отношение (МНО), протромбиновое время] параметров. Однако несмотря на высокую специфичность (98%) прогноза, эта шкала обладает сравнительно низкой чувствительностью (67%) в отношении прогнозирования высокого риска неблагоприятного исхода. Кроме этого, ЛДГ обычно не определяется в районных ЛПУ (стационарах первого и второго уровней), что не позволяет использовать эту шкалу в полном объеме. Данная методика не учитывает также день болезни на момент поступления пациента в стационар, а значит и сроки начала надлежащей терапии КГЛ, что в ряде случаев является критичным для прогноза летального исхода. Шкала имеет только 2 возрастных интервала, причем один из них (от момента рождения до 60 лет) очень широкий и практически не учитывает особенностей физиологии организма в разные периоды жизни, что снижает точность прогноза.
В связи с вышеизложенным целью работы явилась разработка методики оценки риска летального исхода при КГЛ на основе определения в день госпитализации клинико-лабораторных параметров, доступных в стационарах первого и второго уровня.
Материалы и методы
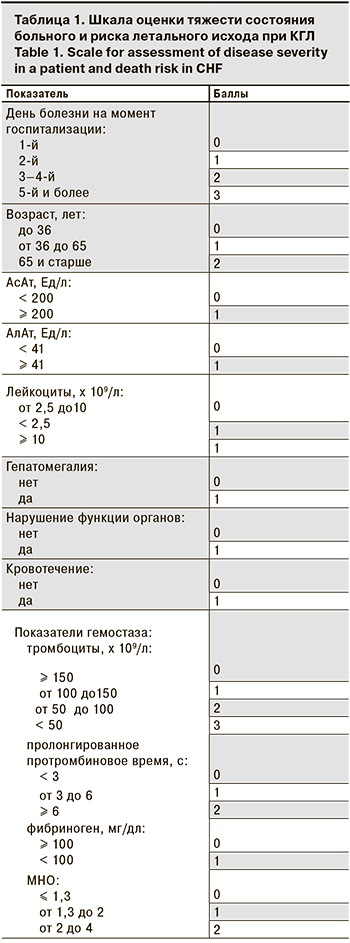
На основании анализа методик оценки тяжести состояния больных КГЛ [10–13] мы разработали собственную шкалу, основанную на 12 параметрах и 2–4 градациях каждого параметра (всего 32 критерия), адаптированную для стационаров первого и второго уровня (табл. 1). Выполнен ретроспективный анализ 52 историй болезни пациентов обоего пола в возрасте от 13 до 67 лет с подтвержденной КГЛ, проходивших лечение в районных ЛПУ Туркестанской (ранее – Южно-Казахстанской) области в период с 2000 по 2018 г. Диагноз был верифицирован на основании обнаружения анти-КГЛ IgM методом ИФА и/или РНК вируса методом ПЦР в реальном времени [14]. Клинические и лабораторные параметры каждого пациента, возраст и сроки госпитализации были оценены в соответствии с разработанной шкалой оценки тяжести состояния больного и риска летального исхода, были подвергнуты сравнению и в дальнейшем послужили основой для разработки шкалы оценки тяжести состояния при КГЛ и риска летального исхода. Полученные данные были подвергнуты статистической обработке.
Использовали методы описательной статистики для относительных величин, критерий χ2, бинарную логистическую регрессию (ROC-кривая).
Результаты и обсуждение
Частота наличия и/или выраженности 10 из 12 (83,3%) критериев оказалась различной у выживших и умерших пациентов (табл. 2).
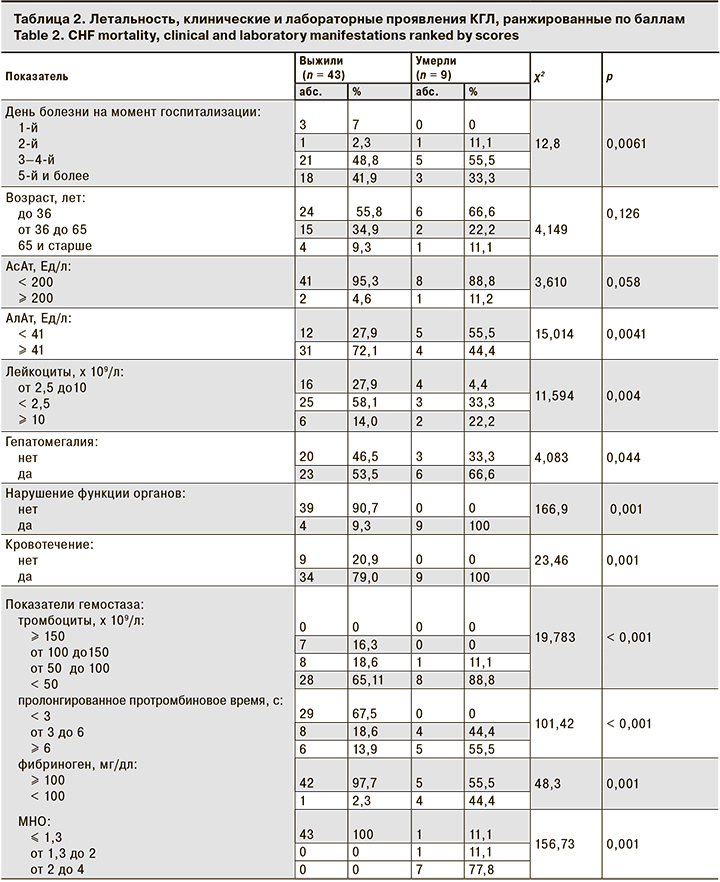
На основании полученных данных была разработана методика прогнозирования исхода КГЛ с использованием балльной шкалы оценки тяжести состояния больных c определением в день госпитализации лабораторных параметров, доступных в стационарах ЛПУ первого/второго уровня.
 Клинические и лабораторные параметры 52 пациентов с КГЛ были соотнесены со шкалой. Каждому параметру было присвоено определенное количество баллов и в дальнейшем определена общая сумма баллов:
Клинические и лабораторные параметры 52 пациентов с КГЛ были соотнесены со шкалой. Каждому параметру было присвоено определенное количество баллов и в дальнейшем определена общая сумма баллов:
- При поступлении в стационар в 1-й день болезни пациенту присваивают 0 баллов, на 2-й день – 1 балл, на 3–4-й – 2 балла, на 5-й и более – 3 балла.
- Возраст пациента моложе 36 лет – 0 баллов, от 36 до 65 лет –1 балл, 65 лет и старше –2 балла.
- Уровень АcАТ < 200 Ед/л – 0 баллов, ≥ 200 Ед/л –1 балл.
- Уровень АлАт < 41 Ед/л – 0 баллов, ≥ 41 Ед/л – 1 балл.
- Уровень лейкоцитов от 2,5 до 10 x 109/л – 0 баллов, < 2,5 x 109/л – 1 балл, ≥ 10,0 x 109/л –1 балл.
- Отсутствие гепатомегалии – 0 баллов, наличие – 1 балл.
- Отсутствие нарушения функции органов – 0 баллов, наличие – 1 балл.
- Отсутствие кровотечения – 0 баллов, наличие – 1 балл.
- Уровень тромбоцитов ≥ 150 x 109/л – 0 баллов, от 100 до 150 x 109/л – 1 балл, от 50 до 100 x 109/л – 2 балла, < 50 x 109/л – 3 балла.
- Протромбиновое время < 3 с – 0 баллов, от 3 до 6 с – 1 балл, ≥ 6 с – 2 балла.
- Уровень фибриногена ≥ 100 мг/дл – 0 баллов, < 100 мг/дл – 1 балл.
- МНО ≤ 1,3 – 0 баллов, от 1,3 до 2 – 1 балл, от 2 до 4 – 2 балла.
Все пациенты были распределены в зависимости от суммы набранных баллов и исхода заболевания (табл. 3), что позволило определить критическое количество баллов для прогнозирования высокого риска летального исхода. При сумме баллов < 11 прогнозировали низкий риск летального исхода КГЛ, при сумме баллов ≥ 11 – высокий риск.
 При сумме баллов ≥ 11 баллов рекомендуется экстренный перевод пациента с использованием транспортировочного бокса для больных с особо опасной инфекцией в стационар третьего уровня для оказания высокотехнологичной помощи в изоляторе, оборудованном для лечения заболеваний, вызванных микроорганизмами I–II групп патогенности. При сумме баллов < 11 больной может продолжить лечение в изоляторе ЛПУ первого/второго уровня c соблюдением медицинским персоналом всех предосторожностей по профилактике ИСМП.
При сумме баллов ≥ 11 баллов рекомендуется экстренный перевод пациента с использованием транспортировочного бокса для больных с особо опасной инфекцией в стационар третьего уровня для оказания высокотехнологичной помощи в изоляторе, оборудованном для лечения заболеваний, вызванных микроорганизмами I–II групп патогенности. При сумме баллов < 11 больной может продолжить лечение в изоляторе ЛПУ первого/второго уровня c соблюдением медицинским персоналом всех предосторожностей по профилактике ИСМП.
Чувствительность, специфичность и прогностическую ценность прогнозирования высокого риска неблагоприятного исхода КГЛ определяли, основываясь на том, что:
- а (истинно положительные результаты) – прогнозируемый неблагоприятный исход (смерть) при сумме ≥ 11 баллов по шкале прогноза исхода КГЛ наступил у 9 пациентов;
- b (ложно положительные результаты) – прогнозируемый неблагоприятный исход (смерть) при сумме баллов ≥ 11 в действительности оказался благоприятным у 1 пациента;
- c (ложно отрицательные результаты) – прогнозируемый благоприятный прогноз при сумме баллов < 11 в действительности ни у одного пациента не оказался неблагоприятным;
- d (истинно отрицательные результаты) – прогнозируемый благоприятный прогноз при сумме баллов < 11 соответствовал действительности у 42 пациентов.
Чувствительность, рассчитанная по формуле:
а/(а + с) x 100% = 9/(9 + 0) x 100% = 100%.
Специфичность, рассчитанная по формуле:
d/(b + d) х 100% = 42/(1+ 42) х 100% = 98%.
Прогнозируемая ценность, рассчитанная по формуле:
a/(a + b) х 100% = 9/(9 + 1) х 100% = 90%.
Полученные данные послужили основой для статистического анализа предлагаемой методики с использованием бинарной логистической регрессии и построением ROC-кривой с площадью (AUC), равной 0,99 ± 0,04 (95% ДИ 0,98–1,0), которая также продемонстрировала высокую чувствительность и специфичность разработанной шкалы (см. рисунок).
Заключение
Результаты проведенного исследования продемонстрировали прогностическую значимость и целесообразность применения данной методики прогнозирования неблагоприятного исхода при КГЛ. Она проста, доступна и обладает бóльшей информативностью по сравнению с разработанными ранее шкалами прогнозирования тяжести и риска летального исхода при данном заболевании.
Предлагаемая методика с высокой вероятностью позволяет прогнозировать развитие неблагоприятного исхода при КГЛ и может использоваться в стационарах первого и второго уровня для оптимизации оказания помощи больным с данной патологией и профилактики ИСМП.



